Recombinant Virus Database
標準AAVベクターを用いた染色体中のAAVベクターコピー数測定法に関する標準操作手順書
- 1. 目的
- 1.1
- 本標準操作手順書は標準アデノ随伴ウイルス(AAV)ベクターを用いて、染色体中のAAVベクターコピー数の測定法について述べたものである。
- 1.2
- 本試験で用いるAAVベクター感染細胞の調製は の記載に従う。
- 1.3
- 本試験で用いるAAVベクターを含むgenomic DNAの調製は の記載に従う。
- 1.4
- 本試験で用いるサーマルサイクラー(MJ Research, PTC-200)の詳細な取扱いは に、デンシトグラフ(アトー, AE-6920M-03型)の詳細な取扱いは に従う。
- 1.5
- 本試験で用いるPCR法によるAAVベクターの高感度検出法はVirus Bank SOP-AAV-001の記載に従う。
- 1.6
- 本試験で用いる標準AAVベクター調製法はVirus Bank SOP-AAV-002の記載に従う。
- 2. 原理
- 2.1
- 標準AAVベクターを用いてPCR法により、標準曲線を作成し、染色体中のAAVベクターコピー数の測定を行うものである。
- 3. 試薬類
- 3.1
- TaKaRa LA Taq(5 U/μl)、10×LA PCR Buffer(Mg2+ Free)、25 mM MgCl2、2.5 mM each dNTP mixture(#RR002A)は宝酒造、分子量マーカー1 kb Ladder(#15615-016)、50×TAE Buffer(#24710-030)、10 mg/mlエチジウムブロマイド溶液(#15585-011)はGIBCO BRL社、アガロース(#A6013)はSigma社製を使用する。
- 4. 標準AAVベクター希釈液の調製
- 4.1
- TA-cloning 法により調製した標準AAVベクターを107から104コピー/μlに段階希釈する。希釈液は用時調製とする。希釈溶液の凍結保存したものを標準液として用いてはならない(DNAのチューブ壁への吸着による感度低下が示唆されたため)。
- 5. 被検サンプルの調製
- 5.1
- 染色体DNA中のAAVベクターコピー数の測定には、標準AAVベクターの検量線の直線領域内で測定できるように段階希釈する。被検サンプルによっては、三段階の10倍希釈系列を作成し予備検討を行う。
- 6. 操作手順
- 6.1
- 標準AAVベクターならびに被検サンプル希釈液1 μlを鋳型として用い、各サンプルは二連でPCRを行う。
- PCRは以下の方法で実施する。即ち、下記の組成の内、Template DNAを除いた49 μlのPCR溶液を200 μl反応用チューブに分注し、1 μlのTemplate DNAを添加する。下記に示すプログラムを設定したサーマルサイクラーによりPCRを実施する。なお、全ての操作において手袋を着用し、試薬類は氷上に置く。
●PCR溶液(1サンプル当たり)

●PCRにおけるサーマルサイクラーのプログラム

- 6.2
- PCR終了後のPCR産物の検出はアガロースゲル電気泳動により実施する。標準AAVベクターと各染色体DNAの希釈サンプルは、同一ゲル上で泳動する。PCR産物5 μlに6×Gel-loading buffer(0.25% bromophenol blue/0.25% xylene cyanol/30% glycerol)を1 μl添加し、そのうちの5 μlをゲルにアプライして1×TAEバッファー中、100 Vで30分間泳動する。
- 6.3
- 終濃度2 μg/mlのエチジウムブロマイドを添加したミリQ水に電気泳動後のゲルを浸し、室温で5分間放置する。その後、水道水で5分間洗浄する。UV(312 nm)照射により、デンシトグラフ(アトー、AE-6920M-03型)にライブ画像を取り込んだ後、解析ソフトウエア「ゾーンデンシトメトリー」により約4 KbのPCR産物のバンドの蛍光強度を定量する。データはExcelのテキストファイルとして保存する。
- 7. 計算
- 7.1
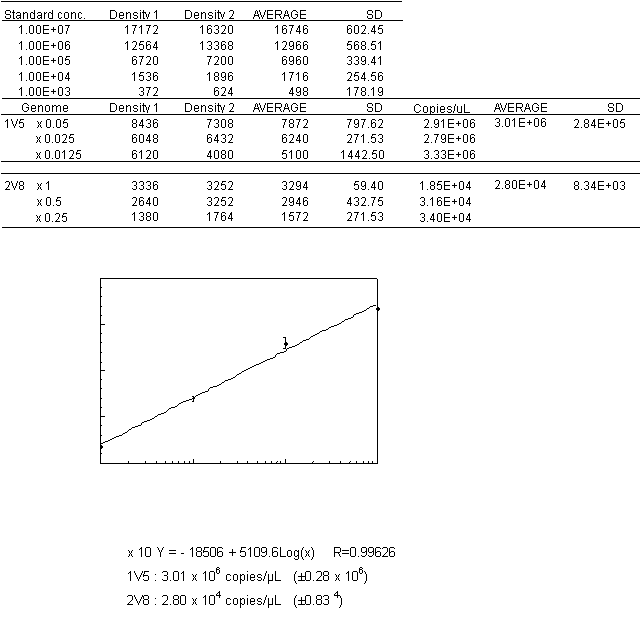
- ゾーンデンシトメトリーによる解析データをコンピューターソフトウエア"Microsoft Excel 5.0"を用いて、コピー数が既知の標準AAVベクターを鋳型として得られるPCR産物の蛍光強度から検量線を作成し、その検量線からAAVベクターのコピー数を算出する。
- 7.2
- プリントアウトし、必要事項を記入し報告用紙とする。
|






