Recombinant Virus Database
PCR法によるMFGレトロウイルスベクター感染細胞(ΨCRIPシリーズ)の組換え遺伝子検出法に関する標準操作手順書
- 1. 目的
- 1.1
- 本標準操作手順書はPCR法によるMFGベクター感染細胞中の、目的の組換え遺伝子の検出について述べたものである。
- 1.2
- 本試験で用いるMFGベクター感染細胞の調製は の記載に従う。
- 1.3
- 本試験で用いるMFGベクター感染細胞ゲノムDNAの調製はVirus Bank SOP-MFG-001の記載に従う。
- 2. 原理
- 2.1
- MFGレトロウイルスベクターはMurine Moloney Leukemia Virus(MMLV)から改造されたものであり、細胞株yCRIPによりパッケージングされる。野生ウイルスのenvの部分に存在するXba I、あるいはNco I切断部位とBamH I切断部位の間に外来DNAが組み込まれている。これらの制限酵素切断部位の上流と下流に両側にプライマーを設定し、外来DNAをPCRで増幅して、特異的に検出する。
- 3. 試薬類
- 3.1
- 滅菌水、10×Ex Taq Buffer、dNTP mixture、TaKaRa Ex Taq(宝酒造)、Mineral oil(Sigma)
- 4. PCRプライマーの調製
- 4.1
- インサートDNA増幅用のprimer #12: 5'-CTTCTCTAGGCGCCCATATG-3'、primer #13: 5'-GCCTGGACCACTGATATCCT-3'は、それぞれ滅菌精製水に終濃度10μMとなるように溶解する。
- 5. 操作手順(操作はすべて手袋をして、氷冷にて行う)
- 5.1
- 1回目のPCR反応液の組成

25 μlのmineral oilで反応液の上を覆って、最高速で2秒間遠心する。
- 5.2
- PCRサーマルサイクラーのプログラム

- 5.3
- PCR終了後のPCR産物の検出はアガロースゲル電気泳動により実施する。泳動ゲルは以下の通り調製する。即ち、ミリQ水で希釈した1×TAE Bufferに懸濁したアガロース(1%、w/v)を電子レンジ等により加熱し、完全にアガロースが溶解したのを確認し、室温で固まらない程度まで冷却する。Mupid-2ゲルメーカーセット(アドバンス、#EM-2)にアガロースを流し込む。大プレート(W 107×L 60 mm)の場合35 ml、小プレート(W 52×L 60 mm)の場合は18 ml使用する。コーム(アドバンス、#COMB25、大プレート25ウェル、小プレート12ウェル)をセットしアガロースが固まるまで放置する。PCR産物5 μlに6×Gel-loading buffer(0.25% bromophenol blue/0.25% xylene cyanol/30% glycerol)を1 μl添加し、そのうちの5 μlをゲルにアプライして1×TAEバッファー中、100 Vで30分間泳動する。
- 5.4
- 終濃度2 μg/mlのエチジウムブロマイドを添加したミリQ水に電気泳動後のゲルを浸し、室温で5分間放置する。その後、水道水で5分間洗浄する。UV(312 nm)照射により、デンシトグラフ(アトー、AE-6920M-03型)にライブ画像を取り込んだ後、PICTファイルとして保存する。バンドのサイズはインサートの長さプラス382 basesになる。
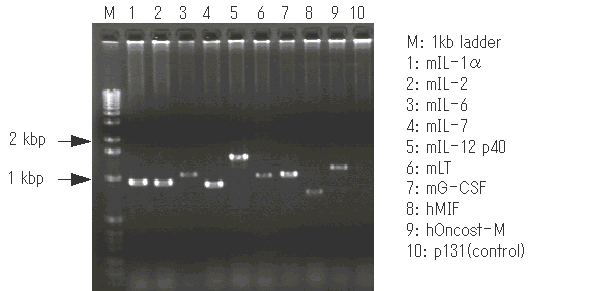
- 5.5
- 測定例を以下に示す。
|






